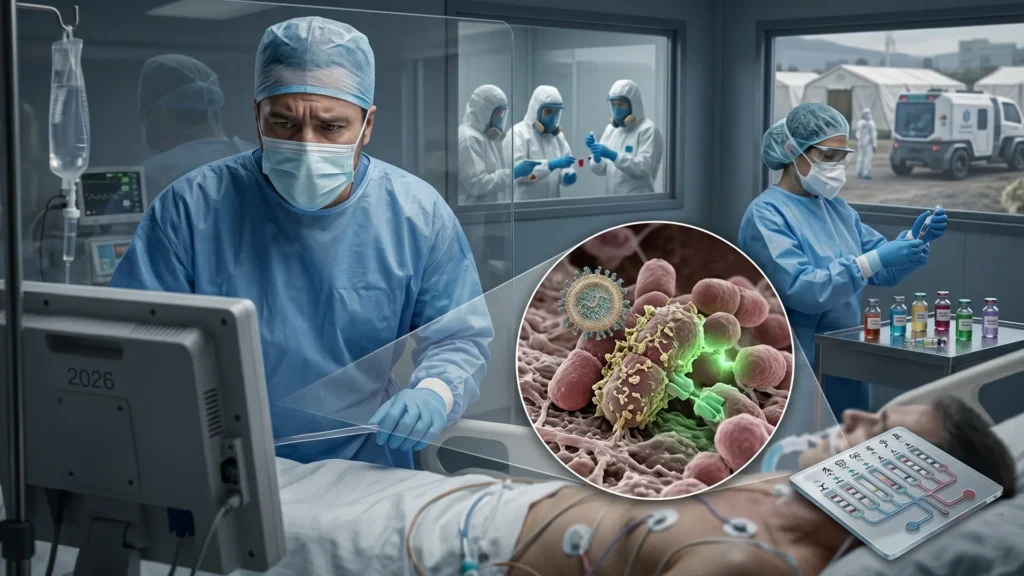
La Organización Mundial de la Salud calificó en 2024 a la resistencia antimicrobiana (RAM) como una de las diez principales amenazas de salud pública global del siglo XXI. Las proyecciones son escalofriantes: si la tendencia actual continúa, para 2050 la RAM podría causar más muertes anuales que el cáncer, con un impacto económico acumulado de 100 billones de dólares globales. Sin embargo, mientras el COVID-19 dominó titulares durante años, esta «pandemia silenciosa» ha recibido una atención mediática mínima, a pesar de matar ya aproximadamente 1.3 millones de personas al año solo por infecciones bacterianas resistentes.
Este artículo hace un corte completo del estado de la resistencia antimicrobiana en 2026: qué superbacterias son las más preocupantes, qué antibióticos nuevos han llegado o están en pipeline, qué estrategias de contención funcionan y por qué el modelo económico actual desincentiva el desarrollo de nuevos antibióticos.
Qué es la resistencia antimicrobiana
La RAM ocurre cuando bacterias, virus, hongos o parásitos evolucionan mecanismos para resistir los fármacos diseñados para eliminarlos. Es un proceso evolutivo natural, acelerado por factores humanos: uso excesivo e inadecuado de antibióticos en medicina humana, uso masivo en ganadería, higiene deficiente en hospitales y cadenas de transmisión internacional por viajes y comercio.
Las bacterias pueden adquirir resistencia por mutaciones espontáneas o por transferencia horizontal de genes de resistencia entre especies. Los mismos mecanismos que llevaron 3 mil millones de años de evolución bacteriana están siendo acelerados dramáticamente por la presión selectiva de los antibióticos.
🔬 INVESTIGACIÓN | La dimensión real del problema
Un estudio publicado en The Lancet en 2022 (actualizado 2024) estimó que en 2019 la RAM causó 1.27 millones de muertes directas y contribuyó a casi 5 millones más, superando a VIH/SIDA y malaria combinadas. Las proyecciones del Reporte O’Neill (actualizado 2023) estiman que para 2050 la RAM causará 10 millones de muertes anuales si no se toman medidas urgentes. El impacto económico acumulado proyectado supera los $100 trillones de dólares.
La lista crítica OMS 2024: los patógenos prioritarios
La OMS publica periódicamente su lista de patógenos prioritarios para desarrollo de nuevos antibióticos. La actualización de 2024 clasifica así:
📊 TABLA CLÍNICA | Patógenos prioritarios según OMS 2024
| Prioridad | Patógeno | Resistencia a | Contexto típico |
|---|---|---|---|
| CRÍTICA | Acinetobacter baumannii | Carbapenémicos | Infecciones hospitalarias, UCI |
| CRÍTICA | Pseudomonas aeruginosa | Carbapenémicos | Hospitalarias, fibrosis quística |
| CRÍTICA | Enterobacterales (E. coli, Klebsiella) | Carbapenémicos, 3ª gen cefalosporinas | Urinarias, sepsis, neumonía |
| ALTA | Mycobacterium tuberculosis | Rifampicina (MDR/XDR) | Tuberculosis multirresistente |
| ALTA | Salmonella typhi | Fluoroquinolonas | Tifoidea |
| ALTA | Neisseria gonorrhoeae | Cefalosporinas, fluoroquinolonas | Gonorrea |
| ALTA | Staphylococcus aureus (MRSA) | Meticilina | Hospitalarias, piel y tejidos |
| ALTA | Helicobacter pylori | Claritromicina | Gástricas |
| ALTA | Enterococcus faecium | Vancomicina | Hospitalarias, endocarditis |
| MEDIA | Streptococcus pneumoniae | Penicilina | Neumonía, meningitis |
| MEDIA | Haemophilus influenzae | Ampicilina | Respiratorias |
| MEDIA | Shigella spp. | Fluoroquinolonas | Diarrea |
Fuente: WHO Bacterial Priority Pathogens List 2024.
Las superbacterias más peligrosas en 2026
CRE (Enterobacterales resistentes a carbapenémicos)
Las infecciones por CRE tienen mortalidad cercana al 50% cuando afectan torrente sanguíneo. Los carbapenémicos eran considerados «antibióticos de última línea» hace una década; la propagación de genes como NDM, KPC y OXA-48 los ha vuelto inefectivos en proporciones crecientes de aislamientos clínicos.
MDR-TB y XDR-TB (tuberculosis multi y extensivamente resistente)
Más de 500,000 casos nuevos de MDR-TB anuales en el mundo. El tratamiento estándar toma 18-24 meses, con medicamentos tóxicos y tasas de éxito apenas del 60%. La aprobación reciente de regímenes más cortos con bedaquilina y pretomanid (2019-2022) fue un avance crítico, pero el acceso global sigue siendo desigual.
Gonorrea pan-resistente
Nueve países han reportado casos de gonorrea resistente a ceftriaxona, el último antibiótico de primera línea. Si esta resistencia se disemina, la gonorrea podría volver al estado pre-antibiótico: una ITS con complicaciones severas sin tratamiento efectivo de primera línea.
Los antibióticos nuevos: el pipeline delgado
Entre 2017 y 2024, la FDA aprobó solo 14 antibióticos nuevos. De ellos, la mayoría son variaciones de clases existentes, no mecanismos verdaderamente nuevos. Algunas excepciones notables:
- Cefiderocol (Fetroja, 2019): cefalosporina con mecanismo «caballo de Troya» mediante quelación de hierro
- Imipenem-cilastatin-relebactam (Recarbrio, 2019): contra Pseudomonas resistente
- Sulbactam-durlobactam (Xacduro, 2023): específicamente para Acinetobacter resistente
- Contezolid (Youxitai, 2024 China): oxazolidinona nueva con menor toxicidad
- Zoliflodacin (en aprobación 2026): primera nueva clase contra gonorrea en décadas
- Gepotidacin (Blujepa, 2025): primera nueva clase oral contra ITU no complicada
Por qué la industria no desarrolla más antibióticos
Es una de las paradojas centrales del mercado farmacéutico moderno: a pesar de la necesidad crítica, la industria ha abandonado masivamente el desarrollo de antibióticos. Las razones:
- Bajo retorno financiero: los antibióticos nuevos se reservan como «última línea» y se usan poco
- Duración corta del tratamiento: 7-14 días vs tratamiento crónico de otros fármacos
- Genéricos baratos dominan el mercado a 2-3 años post-patente
- Resistencia emerge rápidamente, reduciendo valor comercial sostenible
- Grandes farmacéuticas (Pfizer, AstraZeneca, Sanofi) cerraron investigación antibiótica
- Startups de antibióticos (Achaogen, Melinta, Tetraphase) quebraron pese a aprobaciones
Nuevos modelos económicos: subscription y pull incentives
Varios gobiernos están experimentando con modelos económicos alternativos:
- Reino Unido: modelo de suscripción (pagar tarifa anual fija a las farmacéuticas por acceso ilimitado a ciertos antibióticos nuevos)
- PASTEUR Act (EE.UU.): propuesta legislativa similar, aún en debate
- Subsidios directos pre-aprobación (BARDA, CARB-X)
- Premios por hitos de desarrollo
- Mercados garantizados por organismos multilaterales (GAVI-like para antibióticos)
Estrategias de contención: el enfoque One Health
El control efectivo de RAM requiere acciones coordinadas en tres frentes:
- Salud humana: stewardship antibiótico hospitalario, reducción uso inadecuado en ambulatorios
- Salud animal y agricultura: restricción uso como promotor de crecimiento, ya prohibido en UE
- Medio ambiente: reducción de contaminación con antibióticos en aguas residuales
Este enfoque «One Health» es el consenso global pero la implementación real es desigual y lenta.
Lo que puede hacer cada médico
La prescripción antibiótica responsable sigue siendo la palanca más accesible:
- Evitar prescripción en infecciones virales (gripa, bronquitis viral)
- Usar espectro más estrecho posible según sensibilidad
- Completar cursos con duración basada en evidencia (cortos cuando aplique)
- Solicitar cultivos antes de tratamiento empírico cuando sea posible
- Educar pacientes sobre no compartir ni guardar antibióticos
- Reportar casos sospechosos de resistencia a sistemas de vigilancia
La pandemia que necesita atención ahora
La resistencia antimicrobiana no tiene la visibilidad mediática de otras crisis, pero su impacto sostenido a largo plazo podría superar a cualquier pandemia viral reciente. Requiere acción coordinada entre gobiernos, industria, profesionales de la salud, sistemas agrícolas y sociedad civil. Ignorarla es hipotecar el futuro de la medicina moderna. En Actualidad Médica seguimos cubriendo las amenazas sanitarias globales; complementa con innovaciones médicas en 2026 y las farmacéuticas más grandes del mundo en 2026.