Durante más de 20 años, la investigación farmacológica sobre el Alzheimer fue una sucesión de fracasos. Más de 200 moléculas fallaron en estudios fase III, con pérdidas multimillonarias para la industria y frustración creciente en la comunidad médica. Los pocos medicamentos aprobados (donepezil, memantina) apenas mejoraban síntomas sin afectar la trayectoria de la enfermedad. En 2023-2024, esa historia cambió de rumbo: dos fármacos obtuvieron aprobación acelerada y luego tradicional de la FDA, convirtiéndose en los primeros tratamientos modificadores de la enfermedad en casi 30 años.
Este artículo explica qué son lecanemab (Leqembi) y donanemab (Kisunla), cómo funcionan, qué resultados han mostrado, qué efectos adversos serios tienen, y cuáles son las condiciones reales de acceso en 2026. Es información que todo médico de primer contacto y paciente con antecedentes familiares debe conocer.
Por qué tardaron tanto los tratamientos efectivos
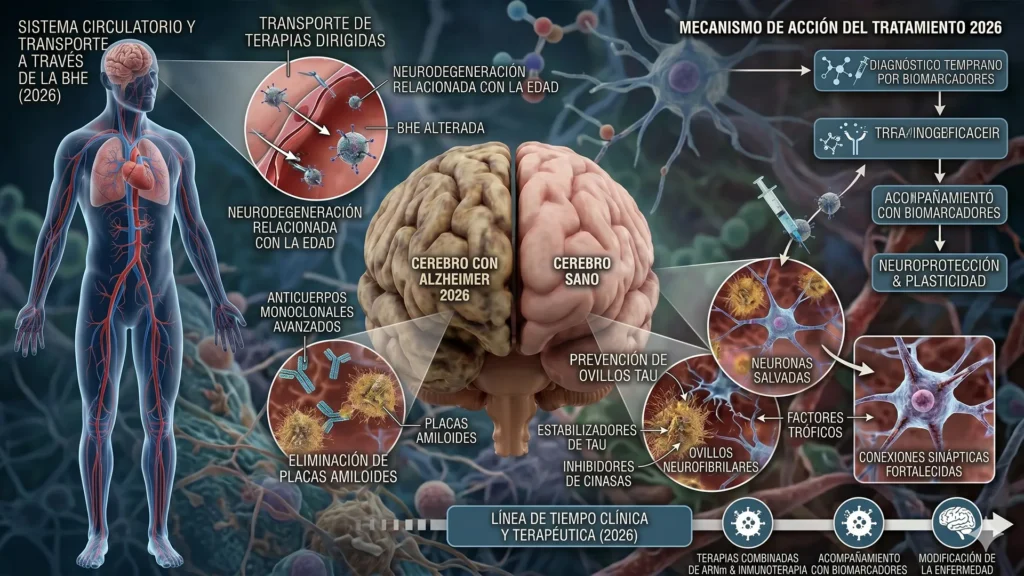
El Alzheimer se caracteriza por la acumulación de dos proteínas anormales en el cerebro: placas de beta-amiloide extracelular y ovillos de tau intracelular. La hipótesis amiloide, dominante por décadas, sostenía que reducir el amiloide debía detener la enfermedad. Múltiples ensayos clínicos fallaron en demostrarlo, generando dudas sobre la hipótesis misma.
El cambio de paradigma llegó al entender dos cosas: primero, los fármacos necesitaban administrarse en etapas mucho más tempranas (deterioro cognitivo leve o Alzheimer leve, no moderado o severo). Segundo, debían eliminar eficazmente las formas oligoméricas del amiloide, no solo placas terminales. Lecanemab y donanemab fueron diseñados con ambos principios.
🔬 INVESTIGACIÓN | Qué dice la evidencia clínica
El estudio Clarity AD (lecanemab, Eisai/Biogen) con 1,795 pacientes mostró reducción del 27% en deterioro cognitivo a 18 meses medido por CDR-SB. El estudio TRAILBLAZER-ALZ 2 (donanemab, Eli Lilly) con 1,736 pacientes mostró reducción del 35% en deterioro cognitivo en pacientes con bajo/medio nivel de tau. Ambos fueron publicados en NEJM y JAMA respectivamente. Es la primera vez en la historia que dos estudios fase III distintos demuestran alteración del curso de la enfermedad en Alzheimer.
Lecanemab (Leqembi) y donanemab (Kisunla) comparados
📊 TABLA CLÍNICA | Comparación de los dos fármacos modificadores aprobados 2026
| Característica | Lecanemab (Leqembi) | Donanemab (Kisunla) |
|---|---|---|
| Compañía | Eisai + Biogen | Eli Lilly |
| Aprobación FDA tradicional | Julio 2023 | Julio 2024 |
| Mecanismo | Anti-amiloide (soluble + placas) | Anti-amiloide (placas maduras) |
| Administración | IV cada 2 semanas | IV cada 4 semanas |
| Duración del tratamiento | Indefinida (continúa si beneficio) | Hasta limpiar placas (6-18 meses) |
| Reducción deterioro a 18m | 27% (CDR-SB) | 35% (iADRS, pacientes bajos tau) |
| ARIA-E (edema cerebral) | ~13% | ~24% |
| ARIA-H (microhemorragias) | ~17% | ~31% |
| Costo anual EE.UU. | ~$26,500 | ~$32,000 |
| Genotipo APOE ε4 homocigoto | Uso con precaución | Contraindicación relativa |
Fuente: FDA approval documents, Clarity AD (NEJM 2023), TRAILBLAZER-ALZ 2 (JAMA 2023), prescribing information 2026.
Cómo funcionan: la cascada amiloide revisitada
Ambos son anticuerpos monoclonales dirigidos contra beta-amiloide, pero con diferencias clave. Lecanemab se une preferentemente a protofibrillas solubles (formas intermedias) y tiene mayor afinidad por amiloide soluble que por placas maduras. Donanemab se une específicamente a una forma modificada del amiloide (N3pG-Aβ) que solo se encuentra en placas consolidadas. Esta diferencia mecanística explica algunos de los patrones distintos de eficacia y efectos adversos.
El tema central de los efectos adversos: ARIA
El nombre técnico es Amyloid-Related Imaging Abnormalities (ARIA), y se divide en dos tipos: ARIA-E (edema cerebral visible en resonancia) y ARIA-H (microhemorragias). Son complicaciones serias que requieren monitoreo estricto con resonancias periódicas durante el tratamiento. La mayoría son asintomáticas pero algunas son graves, y se han reportado muertes atribuibles a estas complicaciones, especialmente en pacientes con genotipo APOE ε4 homocigoto.
La estratificación genética es obligatoria antes de iniciar el tratamiento: pacientes con dos copias del gen APOE ε4 (aproximadamente 2% de la población general) tienen riesgo mucho mayor de ARIA. Esto ha generado un nuevo paradigma en neurología: la farmacogenómica del Alzheimer es ahora un paso previo indispensable.
Criterios para recibir el tratamiento
No todos los pacientes con Alzheimer son candidatos. Los criterios actualmente aplicados:
- Diagnóstico confirmado de Alzheimer con evidencia de amiloide (PET o punción lumbar)
- Deterioro cognitivo leve o Alzheimer en etapa leve (MMSE típicamente 22-30)
- Sin antecedente de hemorragia intracraneal reciente o microhemorragias múltiples en resonancia
- Genotipo APOE conocido y discutido con el paciente para consentimiento informado
- Capacidad de seguimiento con resonancias periódicas (mínimo 4-5 durante el primer año)
- Acceso a infusión intravenosa regular
El acceso en México y América Latina
COFEPRIS aprobó lecanemab en 2024 para uso en México, con requisitos específicos de prescripción por neurólogo o geriatra. En la práctica, el acceso es limitado por tres factores: costo (el tratamiento anual supera los 500,000 pesos mexicanos por año), infraestructura (requiere centros con capacidad de infusión e imagen de alta resolución), y preparación clínica (pocos neurólogos han completado los módulos de entrenamiento específicos).
Actualmente se estima que menos de 200 pacientes en todo México han recibido lecanemab o donanemab. El número crecerá con la llegada de donanemab al mercado mexicano en 2026 y el potencial desarrollo de fondos de copago por aseguradoras privadas.
Lo que viene: la siguiente generación
Los anti-amiloides actuales son solo el inicio. En el pipeline 2026:
- Remternetug (Eli Lilly): siguiente generación de anti-amiloide, administración subcutánea potencial
- Anti-tau: bepranemab y otros dirigidos al otro mecanismo patológico clave
- Combinación temprana amiloide + tau: posible estándar futuro
- Biomarcadores sanguíneos de Alzheimer: p-tau217 ya disponible comercialmente, diagnóstico sin punción lumbar
- Blarcamesine (anavex): dirigido al receptor sigma-1, mecanismo alternativo
- Terapia génica con BDNF (factor neurotrófico): en fase I
Implicaciones para la detección temprana
Si los tratamientos solo funcionan en etapa leve, la detección temprana se vuelve crítica. Esto está impulsando cambios en la práctica clínica:
- Screening cognitivo rutinario en adultos mayores de 65 años
- Biomarcadores sanguíneos para diagnóstico inicial en atención primaria
- Entrenamiento de médicos familiares para detección temprana
- Integración de IA para análisis de patrones cognitivos en registros electrónicos
Un recurso complementario: la inteligencia artificial en el diagnóstico médico 2026 está acelerando este proceso.
El momento más esperanzador en décadas
Lecanemab y donanemab no son cura, y sus beneficios clínicos modestos vienen acompañados de riesgos serios. Pero son los primeros fármacos en alterar realmente el curso de la enfermedad, lo que representa un cambio histórico de paradigma. Para los millones de familias afectadas por Alzheimer, representan esperanza real por primera vez en una generación. En Actualidad Médica seguimos cubriendo avances neurológicos; complementa con salud mental en 2026 y las farmacéuticas más grandes del mundo en 2026.