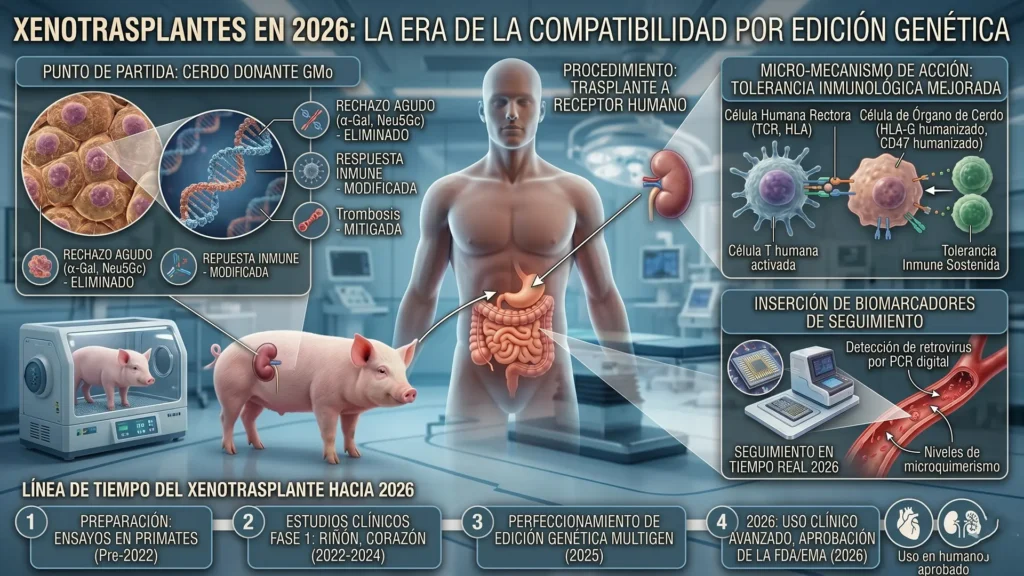
En marzo de 2024, cirujanos del Massachusetts General Hospital realizaron una cirugía que durante décadas fue considerada ciencia ficción: trasplantaron un riñón de cerdo genéticamente editado a Richard Slayman, un hombre de 62 años con enfermedad renal terminal. Fue el primer xenotrasplante de riñón a un ser humano vivo en la historia médica. Unos meses después, en abril 2024, Lisa Pisano recibió tanto un corazón mecánico como un riñón porcino editado. En noviembre 2024 y 2025, nuevos pacientes recibieron intervenciones similares. La era de los xenotrasplantes clínicos en humanos ya comenzó.
Este artículo explica qué son los xenotrasplantes modernos, cómo se logran mediante edición genética CRISPR, qué resultados han mostrado los primeros pacientes, qué compañías lideran el campo y qué significa esto para los más de 100,000 pacientes en lista de espera de órganos solo en Estados Unidos.
La crisis de órganos que justifica el xenotrasplante
Las cifras de la escasez son contundentes: en Estados Unidos hay más de 103,000 personas en lista de espera de trasplante, de las cuales aproximadamente 90,000 esperan un riñón. Cada día mueren 17 personas esperando un órgano. La brecha entre demanda y oferta se ha ampliado en las últimas décadas a pesar de los avances en preservación y asignación de órganos.
El xenotrasplante (trasplante entre especies) fue propuesto como solución teórica desde los años 60, pero enfrentó dos barreras mayores: rechazo inmunológico hiperagudo (ocurre en minutos) y riesgo de zoonosis (transmisión de virus animales a humanos). Ambos parecían insalvables con la tecnología disponible hasta los 2010s
La tecnología de edición genética CRISPR-Cas9, refinada desde 2012, permitió por primera vez editar múltiples genes simultáneamente en el genoma porcino. Los cerdos actuales para xenotrasplante tienen típicamente 10-69 modificaciones genéticas: knockout de antígenos inmunogénicos (como alfa-Gal, Neu5Gc, y Sda), inserción de genes humanos de regulación del complemento y coagulación, y eliminación de retrovirus endógenos porcinos (PERVs). Los cerdos modificados son genéticamente híbridos optimizados para compatibilidad humana.
Los primeros casos humanos documentados
| Paciente | Órgano | Hospital | Fecha | Resultado |
|---|---|---|---|---|
| David Bennett Sr. | Corazón (cerdo, 10 ediciones) | University of Maryland | Enero 2022 | Muerte por falla cardiaca a 60 días |
| Lawrence Faucette | Corazón (cerdo, 10 ediciones) | University of Maryland | Septiembre 2023 | Muerte por rechazo a 40 días |
| Richard Slayman | Riñón (cerdo, 69 ediciones) | Massachusetts General Hospital | Marzo 2024 | Muerte por causas no relacionadas al trasplante a 2 meses |
| Lisa Pisano | Corazón mecánico + Riñón porcino | NYU Langone | Abril 2024 | Rechazo del riñón a 47 días, muerte posterior |
| Towana Looney | Riñón (cerdo, 10 ediciones) | NYU Langone | Noviembre 2024 | Riñón removido a 130 días por rechazo, paciente viva |
| Tim Andrews | Riñón (cerdo, 69 ediciones) | Massachusetts General Hospital | Enero 2025 | En seguimiento al cierre del reporte |
Fuente: Compilación de reportes hospitalarios oficiales, NEJM case reports, y comunicados institucionales 2024-2026.
Las dos compañías líderes: eGenesis y Revivicor
eGenesis (Cambridge, Massachusetts)
Fundada por el Dr. George Church (pionero de la edición genética en Harvard) y Luhan Yang. Desarrolla cerdos «EGEN-2784» con 69 modificaciones genéticas: 59 cambios para inactivar retrovirus endógenos porcinos y 10 modificaciones para mejorar compatibilidad inmunológica. Ha sido la fuente de los riñones trasplantados a Slayman y Andrews.
Revivicor (subsidiaria de United Therapeutics)
Desarrolla cerdos «UKidney» con 10 modificaciones genéticas. Su producto «UHeart» fue el usado en Bennett y Faucette. United Therapeutics ha invertido cientos de millones en construir una instalación de producción de grado clínico para producir cerdos específicamente para xenotrasplantes humanos.
Por qué los riñones tienen más éxito que los corazones (por ahora)
Los primeros casos muestran un patrón interesante: los riñones porcinos están sobreviviendo meses, mientras los corazones fallan en semanas. Varias razones:
- El riñón filtra sin consecuencia fisiológica fatal inmediata si falla parcialmente (hay diálisis)
- El corazón no permite margen de error funcional: cualquier disfunción es letal
- Los riñones tienen menor carga hemodinámica en momentos críticos postquirúrgicos
- El rechazo cardiaco tiene consecuencias más catastróficas e inmediatas
- La inmunosupresión requerida tiene efectos sistémicos que afectan más al corazón
Los retos técnicos pendientes
- Rechazo crónico a largo plazo: los primeros casos aún no permiten conclusiones sobre supervivencia a años
- Regímenes de inmunosupresión optimizados específicos para xenotrasplante
- Monitoreo de zoonosis a largo plazo en receptores y contactos
- Escalamiento de producción de cerdos modificados a volúmenes clínicos masivos
- Regulación internacional coordinada (FDA, EMA, COFEPRIS aún definen marcos)
- Costo: actualmente cada intervención cuesta cientos de miles de dólares
Consideraciones éticas y religiosas
El xenotrasplante plantea preguntas éticas reales que la sociedad debe procesar:
- Uso de animales para órganos humanos: posturas encontradas entre grupos animalistas
- Compatibilidad religiosa: judaísmo e islam, tradiciones con restricciones sobre cerdo, tienden a permitir en caso de pikuach nefesh (salvar vida)
- Consentimiento informado riguroso en contexto donde la alternativa es muerte
- Equidad en acceso si la tecnología se consolida (solo para quien pueda pagar)
- Identidad y aceptación psicológica de vivir con órgano de otra especie
- Trazabilidad y responsabilidad legal si surgen problemas zoonóticos
Otros órganos en pipeline
Más allá de riñón y corazón, están en desarrollo preclínico:
- Hígado porcino: ya trasplantado a humanos con muerte cerebral en China 2024
- Pulmón porcino: fase preclínica en primates no humanos
- Islotes pancreáticos: para diabetes tipo 1
- Piel: para quemaduras severas con mejor compatibilidad
- Córnea: como alternativa a donación humana
Proyecciones 2026-2035
- 2026-2028: ensayos clínicos fase II con múltiples pacientes en EE.UU. y Europa
- 2028-2030: potencial aprobación condicional para pacientes sin alternativa
- 2030-2032: expansión a otros órganos (corazón con mejores resultados)
- 2035: posible incorporación regulatoria plena si los datos a largo plazo son favorables
- Costo: reducción gradual con escalas pero siempre significativo
Una solución potencial para la crisis de órganos
El xenotrasplante no resuelve mañana la crisis de órganos, pero los primeros casos humanos de 2024-2025 demostraron que la tecnología es clínicamente viable, no teórica. Si las próximas décadas traen resultados consistentes a mediano plazo, podríamos ver el fin gradual de las listas de espera como las conocemos. En Actualidad Médica seguimos cubriendo este frente histórico de la cirugía; no te pierdas innovaciones médicas en 2026 e inversión en tecnología médica. Visita https://actualidadmedica.org/